유안펑 POV: EUDAMED의 업데이트 시간표
EU 위원회는 최근 EUDAMED 개정안 2024/1860을 바탕으로 EUDAMED의 완료 및 시행을 위한 업데이트를 발표했습니다.이 기사는 EUDAMED의 현재 일정을 설명하고 산업이 이에 따라 준비하도록 돕기 위해 이러한 일정에 대한 우리의 견해를 설명합니다..
현재 EUDAMED 시간표:
- 기능 EUDAMED 모듈의 첫 번째 의무적 적용의 목표 날짜는 여전히 2026년 1월 1일입니다.감시 모듈은 2026년 3분기부터 의무화 될 것으로 예상되며 EUDAMED의 완전한 기능은 2027년 2분기에 계획됩니다..
- Actor, UDI & Devices, 인증서, 시장 감시 모듈은 현재 감사 중입니다.독립적인 최소 유력 제품 (MVP) 감사는 감사 준비가 된 것으로 간주되는 모듈의 기능과 상호 연결성을 평가하고 확인하는 것을 목표로합니다.이 감사는 2025년 2분기에 완료될 것으로 예상됩니다.
- Mandatory use of each module is to commence six (6) months after the module is declared fully functional through the independent audit and publication in the Official Journal of the European Union (OJEU)액터, UDI & 디바이스, 인증서 및 시장 감시 모듈은 2025 년 2 분기 말까지 완전히 작동한다고 선언 될 것으로 예상되며 1 월 1 일까지의 의무 적용 날짜로 이어질 것입니다. 2026.
- 네 - 액터, UDI 및 장치, 인증서 및 시장 감시 모듈은 2025년 2분기 말까지 완전히 기능적이라고 선언되고 2026년 1월 1일 산업용으로 의무화 될 것으로 예상됩니다.
- 감시 모듈은 현재 진행 중인 MVP 감사의 일부가 아니며 앞서 언급한 모듈과 함께 완전히 작동한다고 선언되지 않습니다.개정된 시간표는 해당 모듈의 감사가 2025년 2분기와 3분기 사이에 이루어질 것이라고 나타냅니다.2026년 2분기에 적용을 의무화하는 것을 목표로 하고 있습니다.
- 네 - 임상 조사/성능 연구 (CI/PS) 모듈의 개발은 2026년 3분기까지 계속될 예정이다.CI/PS 모듈을 평가하기 위한 감사는 CI/PS MVP가 개발되면 나머지 5개의 모듈과 함께 완료됩니다..
- 네
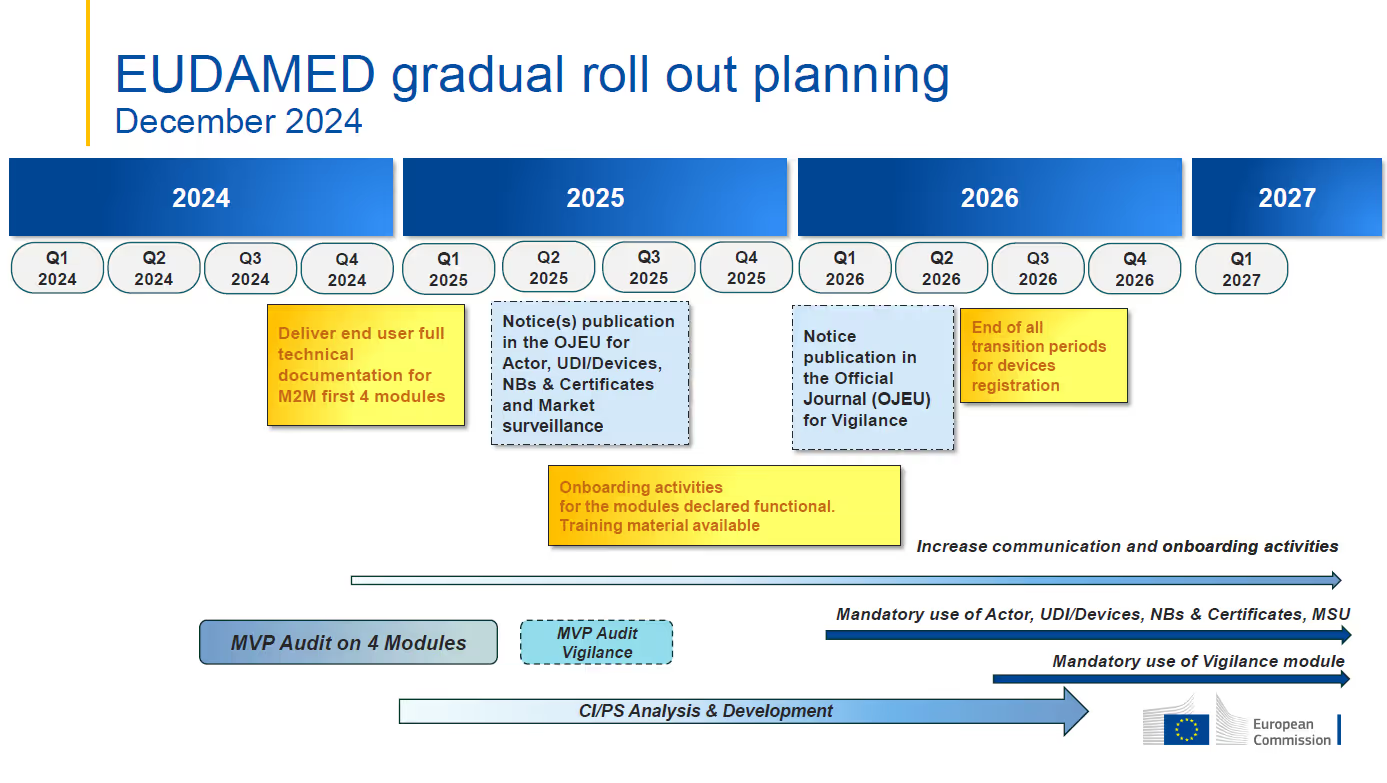
사진:유럽 위원회
EU 위원회는 최근 EUDAMED를 완료하고 실행하기 위한 업데이트를 발표했습니다.수정안 2024/1860이 기사는 EUDAMED의 현재 일정을 설명하고 산업이 이에 따라 준비할 수 있도록 이러한 일정에 대한 우리의 견해를 설명합니다.
현재 EUDAMED 시간표:
- 기능 EUDAMED 모듈의 첫 번째 의무적 적용의 목표 날짜는 여전히 2026년 1월 1일입니다.감시 모듈은 2026년 3분기부터 의무화 될 것으로 예상되며 EUDAMED의 완전한 기능은 2027년 2분기에 계획됩니다..
- Actor, UDI & Devices, 인증서, 시장 감시 모듈은 현재 감사 중입니다.독립적인 최소 유력 제품 (MVP) 감사는 감사 준비가 된 것으로 간주되는 모듈의 기능과 상호 연결성을 평가하고 확인하는 것을 목표로합니다.이 감사는 2025년 2분기에 완료될 것으로 예상됩니다.
- Mandatory use of each module is to commence six (6) months after the module is declared fully functional through the independent audit and publication in the Official Journal of the European Union (OJEU)액터, UDI & 디바이스, 인증서 및 시장 감시 모듈은 2025 년 2 분기 말까지 완전히 작동한다고 선언 될 것으로 예상되며 1 월 1 일까지의 의무 적용 날짜로 이어질 것입니다. 2026.
- 네 - 액터, UDI 및 장치, 인증서 및 시장 감시 모듈은 2025년 2분기 말까지 완전히 기능적이라고 선언되고 2026년 1월 1일 산업용으로 의무화 될 것으로 예상됩니다.
- 감시 모듈은 현재 진행 중인 MVP 감사의 일부가 아니며 앞서 언급한 모듈과 함께 완전히 작동한다고 선언되지 않습니다.개정된 시간표는 해당 모듈의 감사가 2025년 2분기와 3분기 사이에 이루어질 것이라고 나타냅니다.2026년 2분기에 적용을 의무화하는 것을 목표로 하고 있습니다.
- 네 - 임상 조사/성능 연구 (CI/PS) 모듈의 개발은 2026년 3분기까지 계속될 예정이다.CI/PS 모듈을 평가하기 위한 감사는 CI/PS MVP가 개발되면 나머지 5개의 모듈과 함께 완료됩니다..
- 네

사진:유럽 위원회
림시스는 이 발표가 각 이해관계자 그룹에 미치는 영향을 다음과 같이 보고 있습니다.
유안펜
UDI는 주의 모듈과 미래의 상호 작용과 함께 앞장서고 있습니다.림시스는 업데이트된 목표일에도 불구하고 UDI와 시장 감시 후 기능을 계속 개발할 것입니다.우리는 또한 EUDAMED와 기계-기계 (M2M) 역량으로 상호 작용하기 위해 데이터 전송 (DTX) 기능을 구축하는 잠재적 인 영향을 인식합니다.EUDAMED에 필요한 M2M DTX에 대한 최종 요구 사항의 공개와 함께, Rimsys는 EUDAMED 솔루션의 일부로 우리의 연결을 최종화하고 M2M 기능을 제공할 수 있습니다.
산업/고객
유럽 위원회 (EC) 는 EUDAMED 일정을 여러 번 업데이트했기 때문에 산업계는 새로운 목표 날짜를 받아들이는 데 약간의 거부감을 가질 것으로 예상됩니다.이것은 EUDAMED 준비에 대한 재 참여를 지연시킬 수 있습니다.그러나, 우리는 EC가 이 업데이트된 일정을 밀어붙일 것으로 기대하지 않습니다.올해 2분기에 EUDAMED에 데이터를 제출할 계획이 없는 제조업체는 이 기간을 충족시키기 위해 상당한 어려움을 예상해야 합니다.예상 모듈의 감사가 진행되고 관련 기술 문서를 공개하고,림시스 (Rimsys) 는 규제 데이터를 지금부터 조직하고 가능한 모든 EUDAMED 모듈에 정보를 신속하게 제출하기 위해 조치를 취하는 것을 권장합니다..
EU 위원회
유럽연합은 산업이 그 해결책을 계속 개발하고 자발적으로 데이터를 제출하도록 강력히 권고합니다.위원회의 입장은 데이터의 조기 제출은 기업들에게 전 세계 메디테크 산업의 공격에 앞서 데이터를 확보할 수 있다는 장점을 줄 것입니다.EUDAMED가 의무화되는 동시에 데이터를 추가하려고하는 모든 회사입니다. 이러한 회사는 또한 데이터 제출 문제가 발생할 경우 위원회 자원을 사용하여 작업 할 수 있습니다.
* 참고 - 이 문서에는 규제 해석과유안펜우리는 가능한 한 정보를 제공하려고 노력하지만, 이 정보는 규제 당국의 공식 지침을 대체할 목적으로 제공되지 않습니다.

